
▶ 엔지켐생명과학주가
- 현재 원료의약품 의약화학을 기반으로 합성신약을 연구, 개발하고 기술이전 등을 통해 사업화를 이어가고 있음.
- 동물약품, 화학약품, 식품, 건강보조식품, 식품첨가물, 의약품, 의약외품, 화장품을 제조 및 판매하는 사업을 여위함.
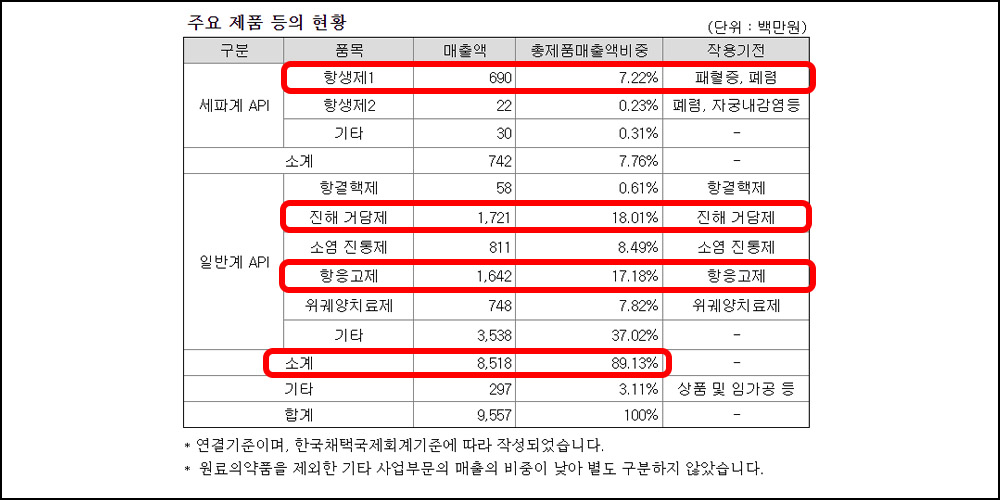
- 세파계API로는 항생제 일반계 API로는 항결핵제, 진해 거담제, 소염 진통제, 항응고제, 위궤양 치료제 등을 제품으로 보유하고 있음.
▶ 8/7. 엔지켐생명과학주가, 미 FDA 코로나 2상 승인 소식.
- 6일(현재 시각)으로 국내 최초로 미국 식약의약국(FDA)로부터 신약물질 'EC-18'에 대한 코로나 10 치료제 임상 2상 시험계획(IND) 승인받았다고 7일에 밝힘.
- 미국이 국내보다 코로나 19 환자 수가 월등히 많고 중증 환자 비율도 높아 임상지원 환자를 모집하기 유리해 이르면 내년 상반기 내엔 임상이 마무리될 것으로 조심스럽게 전망하고 있음. 엔지켐은 임상 경과에 따라 EC-18을 우선 투약할 수 있게 FDA에 긴급 사용승인(EUA)도 신청할 계획.

- 엔지켐생명과학은 FDA가 EC-18이 코로나19 사망요인 1위인 사이토카인 폭풍을 효과적으로 제어하는 작용기 전에 주목해 코로나 19 임상 2상 IND를 신속하게 승인해 준 것으로 분석하고 있음.
- EC-18은 항코로나 19 작용 기전을 검증받은 신약물질. 패턴인식 수용체(PRR, TLRs)의 세포 내 재순환을 촉진시켜 코로나 19로 인한 사이토카인 폭풍 등 염증성 질환을 효과적으로 치료.
- 이번 임상은 코로나 19 감염성 폐렴 환자 60명을 대상으로 다기관, 무작위 배정, 이중맹검, 위약대조 시험이 진행. 환자 30명에게는 EC-18과 표준치료제를, 나머지 위약과 표준치료제를 투약해 경증 폐렴 환자를 대상으로 EC-18이 중증 폐렴 및 급성호흡곤란증으로의 진행을 어느 정도 예방할 수 있는지 효능 및 안전성 평가가 이뤄짐.

▶ 6/24. 엔지켐생명과학주가, 글로벌 신약 특허 등록 100건 돌파
- 미국, 중국, 일본, 프랑스, 독일, 스위스, 영국, 스페인 등 전 세계 20여 개국 특허청으로부터 신약개발과 기술 라이선스에 필수적인 '글로벌 신약' 관련 국내외 특허 총 101건을 등록했음
- 글로벌 신약 EC-18의 기술과 관련해 EC-18 유도체 물질, 제법, First-in-Class(세계 최초) PETA 염증성 질환 치료 작용하기 전, 코로나19 감염병, 항암, 비알콜성지방간염(NASH), 구강점막염, 호중구감소증 등 약 170건의 특허를 확보.

- 글로벌 신약 관련 특허 101건을 포함, 원료의약품 관련 특허 10건, 조영제 관련 특허 2건을 등록해 총 113건의 등록된 특허를 보유. 현재 글로벌 신약 특허 68건과 원료의약품 2건, 조영제 14건 등 총 84건의 특허를 출원한 상태로 연내 150건 이상의 특허를 성취할 것으로 기대.
- 손 대표는 1분기 매출액 대비 연구개발비가 35%를 넘어 코스닥 기업 2위를 차지하는 등 글로벌 신약 개발 기술과 관련 지적재산권 확보에 집중 투자해왔다며 글로벌 바이오 제약기업으로 도약할 것이라고 말했음.
▶ 엔지켐생명과학주가.
- 엔지켐생명과학주가는 최초로 미 FDA 코로나 치료제 2상 승인 소식에 주목을 받고 있습니다. 이 글은 엔지켐생명과학주가 및 기업분석 시 참고해 주세요.



댓글 없음:
댓글 쓰기